案例05:原始记录溯源-临床试验用药/器械保存温湿度记录的监查发现
撰稿人:临床一部 罗梓杰 2020年6月10日
临床试验过程中,研究中心通常会设置GCP药房,并由药物管理员对临床试验用药进行接收、保存、发放与回收等进行管理,临床试验用药保存的条件会有特定的要求,对保管过程需要进行严格的控制。尤其是对于温湿度的要求,一般采用电子温控系统进行管理。

案例背景:
监查员在监查时发现某中心GCP药房保存的试验用药的湿度异常的情况(试验药物要求的温湿度为:常温常湿):
情况1:监查发现试验用药温湿度超标,超湿的最大值为86.5%,首次获知及时汇报申办方沟通,申办方提供药物稳定性说明提示“药物材料有铝塑包装,按之前的稳定性数据(三因素试验),湿度未达90%不受影响,可以继续使用”,之后续密切关注试验用药保存的温控情况,未出现湿度超出90%的情况,
情况2:CRC定期导出温湿度发现个别时间点湿度异常,自行分析其原因为冰箱开门时雾气凝结于温湿度计探头导致湿度超标,未进行汇报;后陆续多次出现该情况仍然认为是短暂现象未引起重视;时隔半月后导出温湿度发现湿度超标次数明显增加,汇报CRA,要求打开冰箱将试验器械取出时发现冰箱底部出现积水,底部4盒试验器械外包装沾湿,最终导致该批次保存的试验器械全部作废不能继续使用。
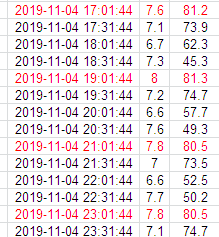
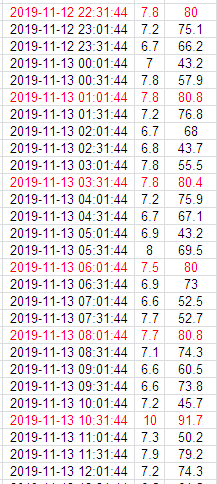
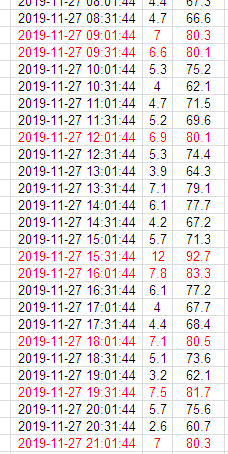
以上案例引发的思考:
1、 如何避免这种情况的出现?
2、 出现后如何正确处理?
案例分享:
1. 情况1监查员在发现试验用药温控超出范围时,能及时做到汇报及沟通处理方案,并最终能获得及时处理提供相关依据信息,使得临床试验能顺利进行,并能意识到后续要密切关注温控的情况,确保保管条件不受到影响;
2. 情况2 CRC和CRA对于器械管理的要求意识不强,发现问题未及时上报,最终导致管理不当浪费了试验器械,造成申办方的损失;
通过以上情况反思,在试验过程中以上情况我们如何避免以及处理:
l 研究单位选择调研:根据试验用药或器械的保存条件,调研研究单位中心药房的保存环境,例如:卫生条件、通风条件、温度情况、人员管理等;包括既往GCP药房的温控记录数据,通过数据分析判断能否符合预期。
l 试验用药或器械提供前的准备:查看GCP药房保存设备的校准、维修、使用记录,是否有相关的稳定性数据(以往的温湿度记录,稳定性报告,自检报告等)能支持保存条件。
l 提前书写试验药物或器械的稳定性说明:与申办方获得药物/器械的相关稳定性数据、说明、报告等,将相关文件递交研究中心备案;
l 制定操作SOP并进行培训:对于试验用药或器械的管理要求制定详细的SOP文件,并对相关人员进行培训,涉及的相关人员必须很熟悉方案及操作SOP;
l 制定项目组团队汇报机制:要求发现任何问题要及时反馈沟通与纠错,确保受试者的安全保障及避免不必要的损失;








