
2025年6月16日,广州海博特医药科技有限公司(简称“海博特”)收到补肾防喘片(2个规格)补充申请批件。截至今日,海博特共为药企申报40余个中成药修改说明书申请,所有审结申请均已获批。这意味着这些品种成功突破“说明书安全信息缺失”的关键瓶颈,具备药品再注册资格。
2023年7月,国家颁布《中药注册管理专门规定》,要求中药说明书【禁忌】、【不良反应】、【注意事项】中任何一项在本规定施行之日起满3年后申请药品再注册时仍为“尚不明确”的,依法不予再注册。
除影响“药品再注册”外,从相关中药政策看,说明书修订亦刻不容缓,不然可能面临进入基药目录受限、调出医保目录、中药品种保护申请困难等情形。
今天距离国家药监局划定的最后期限2026年6月30日,仅剩不到1年。
01 企业困局,为何“尚不明确”难破?
在与数十家中药企业的深度对接中,我们发现核心痛点主要为:
1. 独家品种数据空白:长期未生产品种缺乏临床安全性数据支撑。
2. 文献证据质量薄弱:有效安全性信息稀疏,混杂因素干扰严重。
3. 不良反应术语混乱:缺乏标准化医学编码,临床描述歧义频发。
4. 关键警示信息缺失:毒性成分特殊人群警示未按要求标注。
这些不仅是技术难题,更直接关系批文存续。

【图】参考文献:《已上市中成药说明书安全信息修订实践与思考》
02 持有人主动申请说明书修订技术要求
根据《己上市中药变更事项及申报资料要求》和《已上市中药说明书安全信息项内容修订技术指导原则》要求,中药说明书安全性信息的关键资料为:
1、全面收集安全性证据
·强制提交:国家不良反应监测中心的所有反馈数据(必须完整分析并提交,否则不予批准)。
·延伸检索:本品种的文献、中医理论依据、相近处方药物甚至相关药味的安全性信息等。
2、临床研究是加分项
如果药品上市期间进行了高质量的临床研究,建议在“临床研究”项下也完善相关内容,有益于指导用药,也补充了临床证据,有益于产品市场推广。
目前,说明书修订主要有国家统一修订(本文不讨论)及持有人主动向CDE提出"变更药品说明书中安全性等内容"的补充申请事项这两种途径,后者申报流程如下:
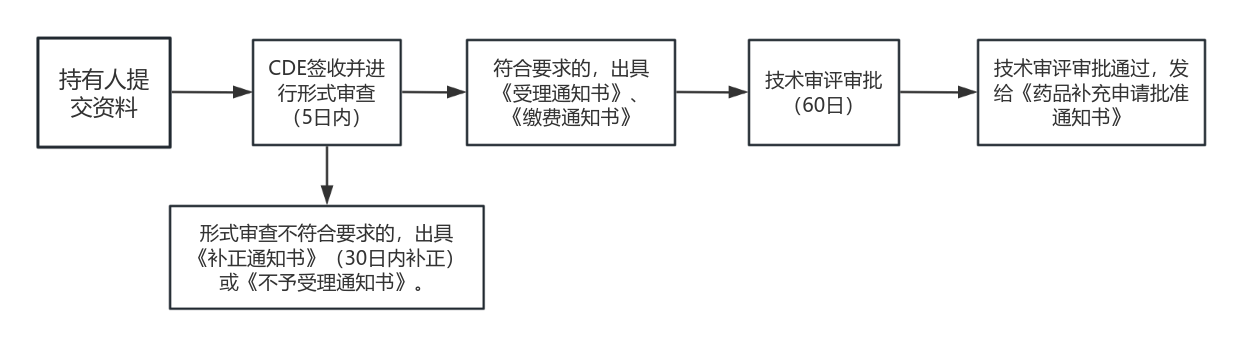
【图】持有人主动修订申报流程
03 海博特全流程解决方案
(一)前期评估:品种梳理与规划
海博特成熟的注册、医学、PV等团队,协助持有中药批准文号的企业(申请人)对自身品种进行梳理,确定哪些品种需要进行说明书修订,并进行优先顺序排列。考量因素如下:
1、对于独家以及市场量大的品种
一般情况下企业需花人力和财力进行系统打造,针对市场反馈、不良反应、生产质量、供应链等问题进行综合评估,提出系统解决方案,分阶段逐步解决。全方位系统修订说明书, 力求系统表征该品种的质量内涵,打造大品种及其品牌。
2、对于在售多年却未有不良反应上报的品种
需要对文献报道的安全性信息进行全面分析,并参考同类产品,总结本品主要不良反应、禁忌和注意事项,并提出说明书修订方案后进行申报。
3、对于市场不大、风险高的鸡肋品种
需要进行全方位评估,针对关键影响因素进行研究,如疗效不明确、适应症宽泛、生产工艺、稳定性等问题要看现有技术和条件能否解决,结合变更管理和修订说明书一并申报。
4、对于未在产在销的品种
需要精准分析评估未生产销售的原因,包括药材资源不能保障, 如市场采购难、涉及濒危动植物,生产工艺、安全性和有效性、不良反应、市场、合规问题等。还有相当一部分中成药因疾病变化、治疗方式改变未再生产和销售,例如含朱砂的小儿制剂,没有再注册的必要,也就没必要进行说明书修订工作。
(二)中期执行:申报资料准备
海博特与药企(申请人)密切沟通,协助申办方根据上述法规及指导原则,收集完整的安全性证据资料,撰写核心资料《安全性相关资料综述》,并完善其他配套技术文件,包括相关证明性文件、立题目的与依据、变更的说明书和标签样稿及对比表、药学(如有)、药理毒理(如有)、临床研究资料(如有)等资料。
此外,根据品种安全性证据完整性,或出于市场拓展、学术推广,以及将来申请“基本药物目录”、“临床指南”做准备的目的,将安全性、有效性、经济性相结合,可开展上市后再评价研究。
(三)后期申报:与CDE沟通直至获批
海博特协助药企(申请人)填写注册申请表,提交申报资料至所在地省级药品监督管理部门,后者在5个工作日内完成申报资料形式审查;药企收到受理及缴费通知书后,需15个工作日内完成缴费。随后CDE审评团队启动时限为60个工作日的审评工作,期间海博特密切跟进审评,及时回应问询,包括与CDE沟通申诉取消不适用的不良反应(如海博特成功申诉删除3个品种肝肾损伤的严重不良反应),直至取得《药品补充申请批准通知书》。
海博特深耕中医药领域15年的国内领先CRO企业,我们有责任以最大的诚意提供最优质的“全程托管型”中药品种修订说明书技术服务,帮助中药企业快速、高效、省心地完成修订说明书工作,从而为企业保护和留存优质中药品种,造福更多的患者,为中医药传承创新的发展贡献力量。
部分资料来源于:国家药监局官网、医药经济报



